食べ物が電池になる!?
レモンに学ぶ蓄電池のしくみ。2026.03.31

レモンに2種類の金属板を差し込んでLEDにつなぐと、小さな輝きを放ちます。「身近な果物が電池になる」、そんな小学校での理科実験を覚えている方もいるのではないでしょうか。なぜ果物に金属板を刺すだけで電気が発生するのでしょうか。そのしくみを探っていくと、私たちが毎日使っている乾電池や家庭用蓄電池のしくみにも通じるものがあります。今回は、身近なレモンを入り口に、電池とは何かを考えてみましょう。
それはキッチンにある“発電所”
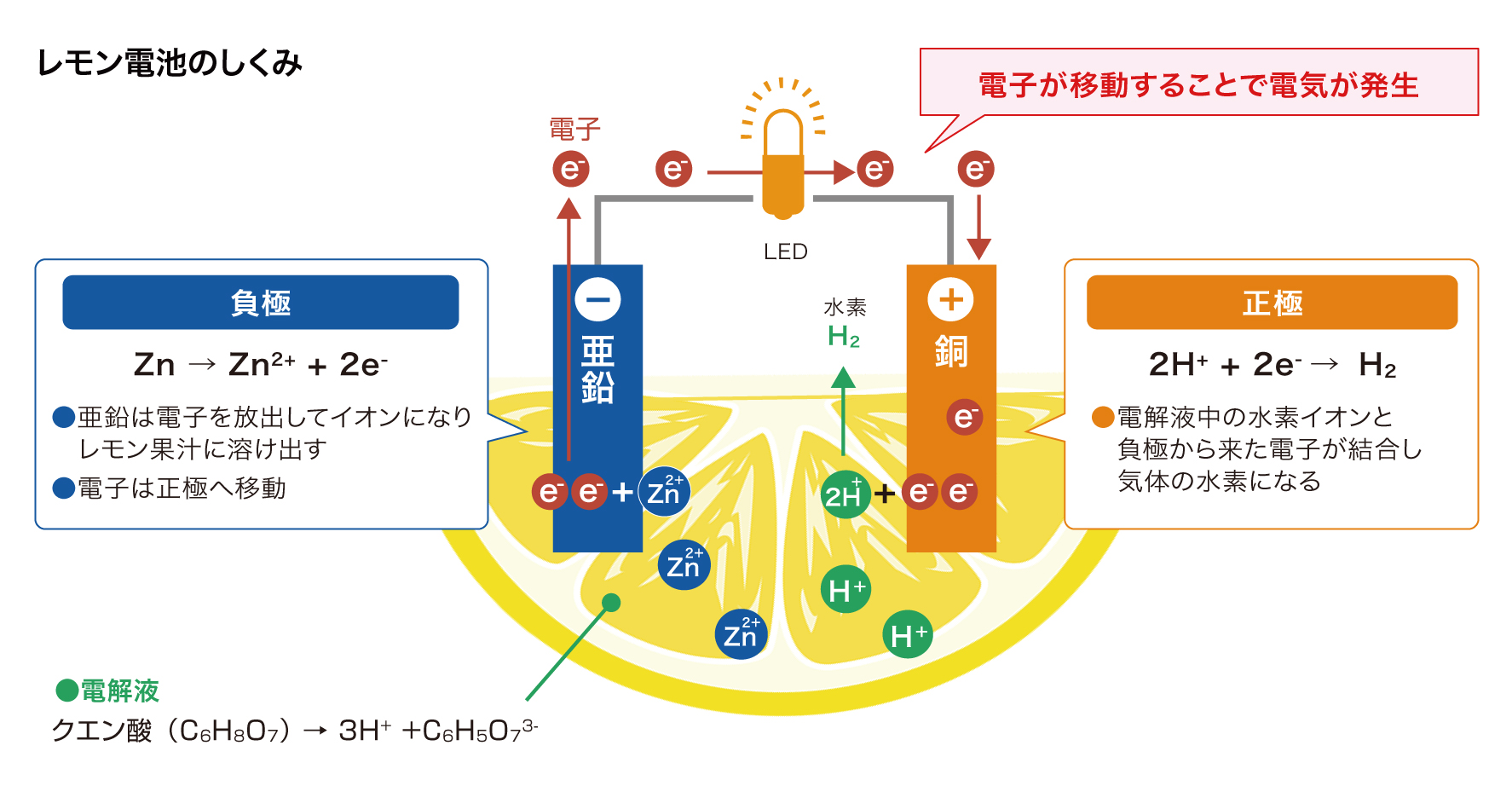
レモン電池の構造はとても簡単です。銅と亜鉛の小さな板を、半分に切ったレモンに刺すだけで電気が発生します。考えてみれば不思議な現象です。
なぜ電気が発生するのでしょうか。理由は大きく二つあります。まず、電極としてイオンになりやすい金属と、なりにくい金属を選んでいることです。中学で習ったイオン化傾向のことです。亜鉛はイオンになりやすく、銅はイオンになりにくい性質があります。
二つ目は、レモン果汁が電解液として働くからです。電解液とは、物質がイオン化して自由に動ける状態にある液体のことで、レモン果汁は主成分であるクエン酸が水に溶けて水素イオン(H+)やクエン酸イオンなどが自由に動ける状態にあります。
こうしたレモン果汁に亜鉛を入れると、亜鉛はたちまち電子を放出してイオン化し、レモンの中に溶け出します。「Zn →Zn2+ + 2e-」
このとき放出された電子が導線を伝わって正極側に移動し、正極のまわりにある水素イオンと結合します。
水素イオンは水素分子(気体)になりブクブクと泡を出して空気中に消えていきます。「2H+ + 2e- →H2」
このように負極で生まれた電子が正極へ移動して消費されることにより、負極から正極へ電子が次々と流れ、それが電流となってLEDを光らせます。
バナナや豆腐、鶏肉も電池になる!?
実は、電池になる食品はレモンだけではありません。オレンジやバナナ、トマト、ジャガイモのほか、意外なところでは豆腐、こんにゃく、鶏肉、さらにはヨーグルトやコーラ、ビールも電池になります。酸っぱいレモンやオレンジは電気が流れるイメージもありますが、その他の食材は電気とは無縁に思えるものばかりです。
電池になるかどうかは「味」ではなく、その食品の中が電解液の状態になっているかで決まります。つまり、水分の中にイオンが溶けた状態で存在していれば電池になる可能性があります。
例えばバナナの中には、水素イオンなどを含むクエン酸やリンゴ酸のほか、さまざまなミネラルが水に溶けた状態で存在します。ミネラルとは金属イオンの総称で、具体的にはカリウムイオンやナトリウムイオンなどです。同じように豆腐にもナトリウムイオンやカリウムイオンなどが含まれています。鶏肉も体液由来のミネラルを含み、これらが電解質として働きます。
こうしたさまざまなイオンがレモン電池の水素イオンなどと同じ働きをすることで、負極から正極へと電子の流れを生み、電気が発生するのです。

実は、乾電池やリチウムイオン電池も基本原理は同じ
では、私たちがふだん使っている本物の電池は、どのようなしくみで電気を発生させているのでしょうか。実は、レモン電池と基本的なしくみは同じなのです。
世界で初めて発明されたボルタ電池は、電極に亜鉛と銅を使い、電解液には希硫酸を使用していました。負極の亜鉛がイオン化し、希硫酸の水素イオンが正極で電子を受け取ることでレモン電池と同様に電気が発生します。
アルカリ乾電池も原理は同じです。電極には亜鉛と二酸化マンガン、電解液には水酸化カリウムが使われています。もちろん、ボルタ電池と違って長期間にわたって安定して電流が流れるようにさまざまな工夫が凝らされていますが、基本的なしくみは同じです。
さらに、スマートフォンや家庭用蓄電池などに不可欠なリチウムイオン電池も、構造はかなり複雑になりますが、基本原理は同じです。正極にはコバルト酸リチウムなどのリチウム遷移金属酸化物、負極にはリチウムを含むグラファイト(炭素)が使われ、電解液は有機溶媒にリチウム塩(LiPF6など)を溶かしたものが使われます。
ただしリチウムイオン電池には、他の電池と決定的に違うポイントがあります。それは充電ができることです。他の電池は電気を生み出す際に電極の亜鉛が溶けたり、電解液の水素イオンが気体になって消えてしまうなど、電池の材料が不可逆的に変化してしまうため元の状態に戻すことはできません。では、なぜリチウムイオン電池だけが繰り返し充電ができるのでしょうか。
なぜリチウムイオン電池は充電できるのか?
リチウムイオン電池は、その名の通りリチウムが大きな役割を果たします。リチウムはイオン化傾向がとても高く、イオンになりやすい物質です。そのためリチウムイオン電池の中でも、金属リチウムではなくつねにリチウムイオン(Li+)と電子(e-)に分かれて存在しています。
例えば、リチウムイオン電池の負極にはグラファイトとリチウムが使われていますが、両者は化学的に結合しているわけではなく、炭素原子による六角形の網目構造の中にリチウムイオンが入り込んだ形になっています。また、正極のコバルト酸リチウム(LiCoO2)という化合物の中でも、リチウムはイオンとして存在しています。
この状態で正負の電極をつないで放電すると、負極にたまっていた電子とリチウムイオンが正極に移動を始めます。電子は導線を通って移動し、リチウムイオンは網目構造から抜け出て電解液の中を移動して正極の中にイオンのまま組み込まれます。
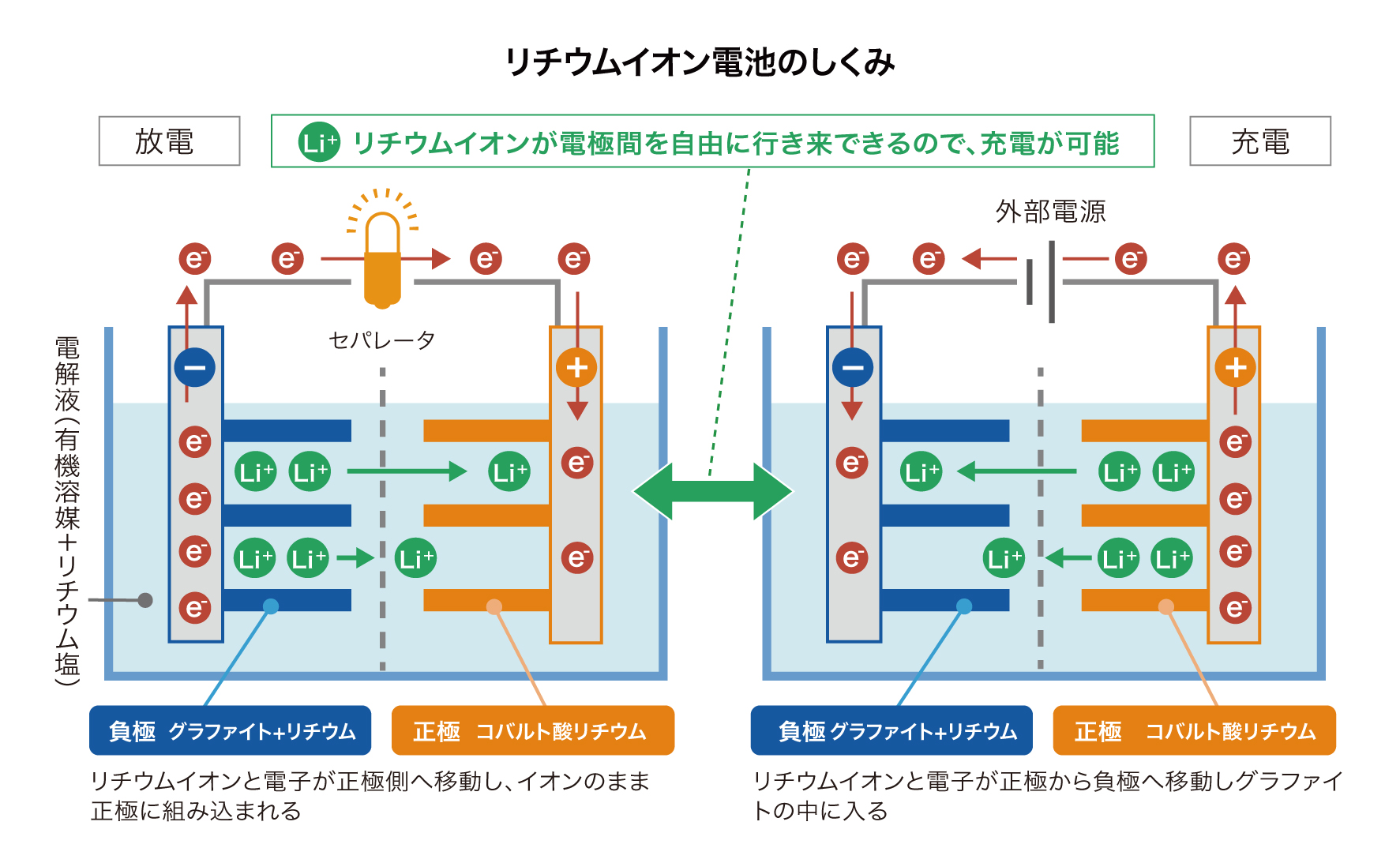
次に、充電するために外部電源をつなぐと、今度はリチウムイオンと電子は負極側に移動します。これによってリチウムイオンと電子がもとの状態に戻り、再び電池として使えるようになるのです。
つまりリチウムイオン電池は、リチウムが化学変化を起こさずにイオンのまま電極間を自由に移動でき、電極や電解液も大きく変化しないので長期間にわたって繰り返し充電ができるのです。
ボルタ電池が発明されてから約200年。電池は大きな進化を遂げました。しかし、レモンに金属を差し込むと小さなあかりが灯る。その驚きは今も変わらない電池の原点です。そう考えると、電池は特別な技術というより、自然の働きを生かした知恵の積み重ねのように思えてきます。レモンから始まる物語が、私たちの暮らしを支える蓄電池につながっている。そのつながりに気づくと、電気が少しだけ、身近な存在に感じられるのではないでしょうか。
出典・参考文献
○NGKサイエンスサイト くだものや野菜で明かりがつく!
https://site.ngk.co.jp/lab/no22/
○Jパワー 食べ物で発電
https://www.jpower.co.jp/plus/contents03/
○古河電池 リチウムイオン電池の構造・仕組み・種類
https://corp.furukawadenchi.co.jp/ja/news/news-20240717.html


